I en centimeter av noe i bilen er det gjerne 100 millioner atomer. Altså har du noen millioner der. Og i kroppen. Minst. Så: Hva er et atom? Som først bare var gass …
Bildet øverst: Etter behandling blir jern til stål som blir biler – rødt er ultra høyfast, gult er høyfast (HSLA); det oransje i nesa er ekstra høyfast for å ta opp smellen mens det røde i buret er supersterkt. Resten er karbonstål – det grønne er legert aluminium. Og alt kom fra detonerende stjerner … (Foto: Volvo)
Av Stein Bekkevold
Navnet kommer av gresk a-tomos, a betyr ikke – altså ikkedelelig – og kjernen består av protoner og nøytroner. Og disse består av kvarker. Rundt kjernen snurrer elektroner – som en sky. Kjernens protoner er positivt elektriske og nøytronene er negative; det var en skummel storm av slike – fra en eksplosjon i rommet et sted – som satte 6000 Airbus-fly på bakken i november.
Kjent kjemisk energi kan ikke spalte kjernen, men innholdet kan dras ut om den bombarderes med partikler. Da har vi fått et annet grunnstoff; slik ble alle stoffer dannet, i kjerneeksplosjoner under enorme trykk og temperaturer – i detonerende stjerner, supernovaer, røde kjemper og det som verre var, noe som fortsatt skjer.
Først var alt bare urgassen hydrogen (hvor kom den fra?) som så ble helium – og så støv, karbon, silisium, nikkel, kobolt og jern fra stjerner og supernovaer, pluss mer karbon fra de røde kjempene, og så kom alt det andre, som oksygen – det hele er jo et mirakel …
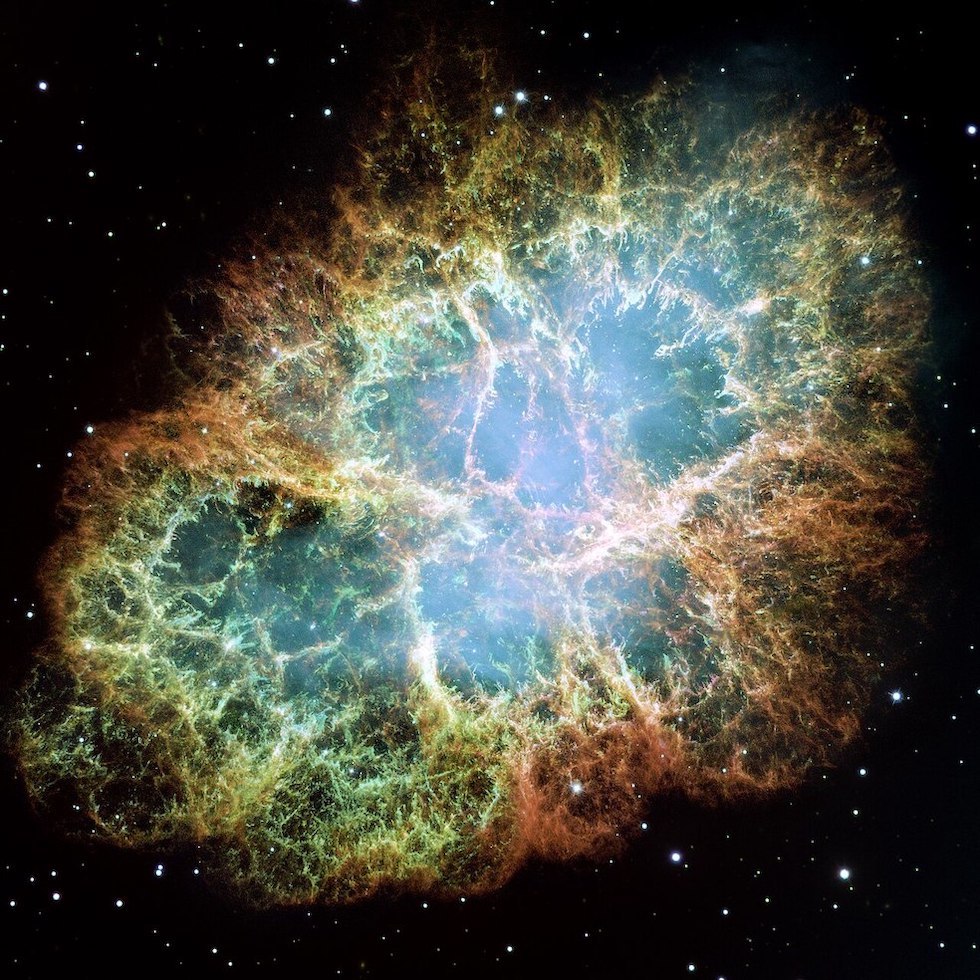
I denne enorme stjernehop blir det stadig født atomer som blir noe annet – av urgassen hydrogen, som blir karbon og jern. Og gull … dette er Krabbenebulosen. (Foto: NASA)
Kvarker
er sammen med leptoner (som elektroner) de minste byggesteinene vi vet om – punktformede elementærpartikler som aldri opptrer alene; de danner par eller tripletter som vi ser i detektorer. Protoner og nøytroner har tre kvarker hver. Elektroner har ingen.
Protoner og nøytroner kalles nukleoner. Et proton og et nøytron har nesten lik masse. Mengden protoner styrer kjernens elektriske ladning – og hvilket grunnstoff atomet utgjør. Antallet protoner er lik atomnummeret i periodesystemet. Og kjernen i grunnstoff kan ha ulike antall nøytroner. Derfor kan ett og samme grunnstoff ha forskjellige isotoper med lik kjemi.Men massetallet er ulikt, så noen egenskaper kan være ulike. Du verden!
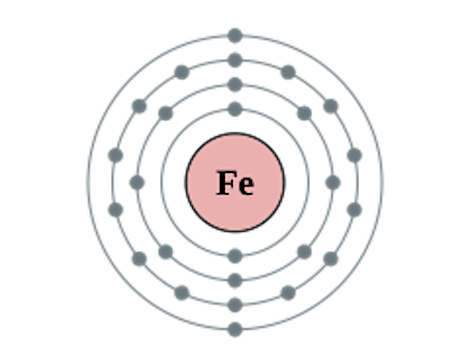
Et jernatom omgitt av sin elektronsky. (Materialteknisk lærebok)
Massen er i kjernen
Rundt en nøytral atomkjerne snurrer samme antall elektroner som antall protoner i kjernen. Dette avgjør stoffets egenskaper. Et viktig poeng er at protoner og nøytroner har like stor elektrisk ladning, men med motsatt fortegn. Denne kalles elektrisk elementærladning, og skrives e.
Nesten all masse i et atom er i kjernen. Elektronene er bare 1/1000 av det hele. Og om du lurer på hva kjerne og snurringer blir til? I ett atom Fe blir de jern, i et Al-atom blir de aluminium – og så videre. Underlig! Det var dagens raske atomteori. Nå vet du hva bilen (og du + universet) består av. Vel bekomme!
PS:
Om du lurer på hva som holder metallene så hardt sammen: Stål er et jernmetall. Styrken (fastheten) i metaller kommer av de kjemisk/metalliske bindingene mellom atomene. Kjemiske bindinger er kreftene – «limet» – som holder alt sammen og skaper stoffet. Partiklene kan være atomer, ioner eller molekyler. Kjemiske bindinger er tiltrekning mellom positive og negative ladninger – elektrostatikk. Hvor sterk den er, avhenger av størrelsen på tiltrekningen.
Kjemiske bindinger kan være sterke eller svake. De sterke virker innover i et molekyl, et metall eller en ion-forbindelse. De kan være metallbindinger, ionebindinger eller kovalente bindinger, det de kaller elektronparbinding. Ionbinding ser vi i salter, kovalent binding inne i molekyler og metallbinding faktisk i metaller. Det er ingen fast overgang mellom dem, en binding kan godt være en mellomting.

Under jernalder og vikingtid utvant vi jern fra elveosene, der malmmyra munnet ut i bekken. (Foto: NGU)
Trekkraft
Atomer har til overmål en elektronegativitet som sier hvor sterkt det kan trekke i elektroner. Forskjellen kan vise bindingstypen. Metallbindinger er det mellom atomer med lav elektronegativitet. Vi kan si at de har en elektronsky av positivt ladde metallioner. En viktig egenskap er at vi kan forskyve disse atomene innbyrdes uten å svekke bindingene, dette gjør at metaller kan deformeres – de er formbare. Elektronskyen forklarer også hvorfor metaller ikke er gjennomsiktige, og stopper varmestråling, mikrobølger og radiobølger, hvorfor de har glans, og at de så godt leder strøm og varme. Også når metaller oksideres – de avgir elektroner og positive ioner, kan vi faktisk forklare rust/korrosjon på bilen med det dumme som hender i «skyen».
Der kan du se! Og alt dette har du både i bilen og i kroppen …

